Электролитные нарушения и их коррекция
C. Давыдова, кандидат медицинских наук, И. Комиссаренко, доктор медицинских наук, Городская клиническая урологическая больница No 47, ЦНИИ гастроэнтерологии, Москва

Клинические состояния, при которых нарушается электролитный гомеостаз, весьма распространены. Нарушения концентрации электролитов при заболеваниях желудочно-кишечного тракта могут возникать при рвоте, аспирации содержимого желудка через зонд, при диарее, кишечных свищах, после обширных резекций кишечника, при синдроме короткой кишки, в пред-, интра- и послеоперационном периодах (их причины: промывание желудка, ограничение приема жидкости перед операцией, прием стероидов, мочегонных, слабительных и других препаратов, влияющих на водно-электролитный обмен, потери внеклеточной жидкости в третье пространство, испарение с поверхности операционной раны и др.). При изучении последствий различных объемов резекции кишечника выявлено, что из объемных операций наименее метаболически агрессивны большие резекции кишки с сохранением баугиниевой заслонки (изолированные тонкокишечные с сохранением илеоцекального угла, левосторонние гемиколэктомии, резекции поперечной ободочной кишки). При анализе лабораторных показателей наименьшие сдвиги выявлены при резекциях поперечной ободочной кишки; они наблюдаются лишь в раннем послеоперационном периоде и затем постепенно, в течение 1–2 лет, становятся преходящими [1]. Более заметны электролитные и белковые нарушения при больших резекциях тонкой кишки. При субтотальных резекциях кишки отмечаются проявления диарейного синдрома, синдрома нарушенного всасывания – СНВ (особенно если удалена илеоцекальная область). У больных с суперкороткой кишкой сдвиги в балансе калия и магния выражены очень сильно. У этой категории больных, независимо от характера патологии, приведшей к столь калечащим операциям, в отдаленном периоде (сроки наблюдения до 1 года и более) отмечен низкий уровень калия (в меньшей степени – магния) даже в плазме крови. Нарушения обмена калия и магния также встречаются при заболеваниях эндокринной системы (гипокалиемия – при диабетическом кетоацидозе, гипокалиемия и гипомагниемия – при гиперосмолярном гипергликемическом некетоацидотическом синдроме, гиперкалиемия – при острой надпочечниковой недостаточности), сердечно-сосудистой системы (гипокалиемия – при застойной сердечной недостаточности и отеке легкого), при почечной недостаточности (гиперкалиемия и гипермагниемия), при панкреатите (гипокалиемия и гипомагниемия), печеночной недостаточности (гипокалиемия и гипомагниемия), при ожогах (гиперкалиемия) и др. Ионы калия содержатся преимущественно внутри клетки, поддерживая поляризацию клеточных мембран, стимулируя активность многих ферментных систем, в частности систем, участвующих в синтезе АТФ, гликогена, белков, ацетилхолина и пр. Недостаточное содержание калия в организме возможно при применении некоторых мочегонных средств, особенно тиазидов или диакарба, гормональных препаратов (гидрокортизона и пр.), при интоксикации сердечными гликозидами и т.д. Гипокалиемия может развиться после введения препаратов инсулина, увеличивающего проникновение иона калия в клетки. Гипокалигистия (уменьшение содержания калия в тканях) может быть при генерализованной или локальной гипоксии даже в случае нормальной концентрации калия в плазме крови: сокращение образования АТФ нарушает возврат калия в клетку. Понижение уровня калия <3,5 ммоль/л сопровождается определенной симптоматикой, и его расценивают как гипокалиемию. Ее основные проявления связаны с нарушением электрических свойств мембран возбудимых тканей. Магний является метаболическим кофактором во многих ферментативных реакциях, связанных, в частности, с утилизацией энергии организмом. Он необходим для нормального функционирования натрий-калий-АТФазного и кальций-АТФазного насосов. Кроме того, магний участвует в контролировании баланса внутриклеточного калия. В гастроэнтерологической клинике основные проблемы, связанные с недостаточностью магния, обусловлены синдромом нарушенного всасывания. Всасывание магния может происходить во всем кишечнике вплоть до сигмовидной кишки, однако в основном он абсорбируется в зоне двенадцатиперстной кишки. При постгастрорезекционных синдромах после дистальных резекций желудка, операций на двенадцатиперстной кишке и в зонах, ее регулирующих, расстройства обмена магния проявляются достаточно очевидно, особенно в отдаленном периоде. С учетом того, что магний элиминируется почками, становится понятным основной механизм возникновения гипермагниемии при почечной недостаточности и частично при гепаторенальном синдроме у больных, перенесших неотложные вмешательства на органах брюшной полости [1]. Учитывая значимость ионов калия и магния в развитии патологии в организме, необходимо проводить коррекцию калий-магниевого дефицита. При этом сочетание ионов калия и магния в одном препарате предпочтительно, так как обосновано тем, что дефицит калия (особенно при заболеваниях желудочно-кишечного тракта – ЖКТ) часто сопровождается дефицитом магния и требует одновременной коррекции содержания в организме обоих ионов. При одновременной коррекции уровня этих электролитов наблюдается аддитивный эффект. Существует ряд препаратов, которые облегчают поступление калия в клетку и этим ускоряют ликвидацию гипокалигистии. Таким свойством обладают инсулин с глюкозой (например, 250 мл 5% раствора глюкозы, 30 мл 2% раствора калия хлорида и 8–10 ЕД инсулина). Особенно эта смесь показана при нарушениях деятельности сердца, внутриклеточном ацидозе. При гиперволемии и гипергидратации применяют смесь, состоящую из 100 мл 10% раствора глюкозы, 2 ЕД инсулина, 4 мл 7,5% раствора калия хлорида и 1 мл 10% раствора кальция глюконата. К препаратам калия относится Панангин, представляющий собой комбинацию аспарагината калия и магния. Калий и магний – два элемента, необходимые для нормальной жизнедеятельности всех клеток организма человека. Их недостаток приводит к развитию и прогрессированию многих заболеваний, особенно болезней сердца и сосудов [2, 3]. Чаще всего мишенью гипокалиемии становится сердечно-сосудистая система. При гипокалиемии могут проявляться такие неспецифические симптомы, как усталость, потеря аппетита, утрата концентрации, апатия, беспокойство, спутанность сознания (до коматозного состояния). Типична периферическая полинейропатия – парестезии в области конечностей, угасание сухожильных рефлексов, а также адинамия. Гипокалиемия ведет к атонии ЖКТ, снижению перистальтики кишечника с постоянными запорами, вплоть до паралитической кишечной непроходимости. Что же касается метаболизма, то могут возникнуть алкалозы и пониженная толерантность к гликозидам [4]. На ЭКГ отмечаются такие изменения, как уплощение Т-зубца, линии слияния TU, снижение сегмента ST, отрицательные зубцы Т, удлинение интервала PQ, появление нарушений ритма сердца: суправентрикулярная и желудочковая экстрасистолия, трепетание и мерцание предсердий – особенно у дигитализированных пациентов [5]. Проведенные исследования выявили уменьшение сердечно-сосудистых осложнений у пациентов с нормальным уровнем калия. Так, А. Ascherio и соавт. [6] в течение 8 лет обследовали 43768 мужчин в возрасте 40–75 лет при отсутствии у них в анамнезе кардиальной патологии и сахарного диабета. Риск смерти от инсульта при приеме большого количества калия значительно понижался (различия достоверны). В других исследованиях при изучении в качестве одной из причин формирования гипокалиемии назначения диуретиков выявлена отрицательная динамика со стороны сердечно-сосудистой системы, что подтверждало сделанные ранее выводы.H. Cohen и соавт. при длительном наблюдении (в среднем 6,7 года) за больными, страдающими артериальной гипертензией – АГ (7563 пациента), из которых 1679 получали диуретики, отметили, что формировавшаяся при этом гипокалиемия (<3,5 ммоль/л) сопровождалась нарастанием частоты сердечно-сосудистых осложнений. Проведенные исследования подтверждают также, что у больных с АГ повышение уровня калия в крови сопровождается более выраженным снижением АД и риска развития нарушений мозгового кровообращения [7]. Оценку изменения содержания калия в крови нецелесообразно проводить отдельно от показателей магния, который является важным кофактором как усвоения калия, так и обеспечения его оптимального внутриклеточного уровня. Так, еще в 1992 г. было доказано [8], что одновременный дефицит калия и магния может приводить к гипокалиемии, резистентной к лечению, если не осуществлять коррекцию дефицита магния. Согласно результатам исследования The Atherosclerosis Risk in Communities (ARIC), гипомагниемия сопровождает развитие ишемической болезни сердца. Наблюдали 13 922 пациента на протяжении 4–7 лет с учетом вредных привычек, уровня холестерина, фибриногена и других факторов [9]. Известно также, что наиболее выражен дефицит магния в случае повышенного содержания атерогенных липидов [10]. Доказано, что у пациентов с эссенциальной АГ в плазме крови понижена концентрация магния, калия и повышена – натрия [11]. Считается, что ионы магния тормозят активность ренин-ангиотензин-альдостероновой системы (РААС) и при их дефиците создаются более благоприятные условия для системной вазоконстрикции [7]. Дефицит магния связан также с нарушенной толерантностью к глюкозе [12] и наличием сердечной недостаточности. Магний задействован и при фибрилляции предсердий. При длительном приеме сердечных гликозидов возникает гипомагниемия, которая вызывает нарушения ритма сердца. В этой ситуации оправданно назначение магнийсодержащих препаратов [13, 14]. Также препараты магния назначают для лечения аритмий, спровоцированных дигиталисной интоксикацией [15], в связи с тем, что функция калий-натриевой помпы восстанавливается под воздействием ионов магния.
Препараты калия и магния в кардиологической практике
Во всем мире препараты калия и магния приобретают все большее значение в качестве терапевтического средства, поскольку они эффективны, практически лишены побочных действий и экономически доступны. Панангин – лекарственный препарат, содержащий калий и магний, позволяет быстро восстановить содержание этих важных элементов в крови, оказывает защитное действие на сердце и сосуды, предупреждая развитие жизнеопасных аритмий, уменьшая токсическое влияние некоторых лекарственных препаратов, улучшая диастолическую функцию сердца, восстанавливая функцию эндотелия, замедляя развитие атеросклероза и снижая риск тромбообразования [16].
Панангин в лечении суправентрикулярных тахиаритмий у больных урологического профиля.
Пониженное поступление с пищей калия и магния, а также избыточное употребление солей натрия – отличительная черта современной цивилизации, что является одним из факторов, способствующих распространенности сердечно-сосудистых заболеваний [8]. Низкое содержание калия и магния повышает риск развития опасных нарушений сердечного ритма и обусловливает неблагоприятный прогноз при сердечной недостаточности [17, 18]. Клинические исследования показали, что аритмии у больных инфарктом миокарда с уровнем калия в крови >4,6 ммоль/л развивались намного реже [19, 20]. Дефицит магния в крови также обусловливает опасные нарушения сердечного ритма. Наиболее типичный вариант аритмии при дефиците магния – желудочковая тахикардия под названием пируэт – грозное состояние, переходящее в фибрилляцию желудочков и при отсутствии лечения приводящее к смертельному исходу [17, 21]. За урологической помощью обращаются преимущественно мужчины пожилого возраста, страдающие заболеваниями как органов мочеполовой системы, так и сердечно-сосудистыми. Нередко у данной категории больных в послеоперационном периоде развиваются суправентрикулярные нарушения ритма сердца. Нами оценена эффективность препарата Панангин в комплексной терапии для лечения и профилактики аритмий у 300 мужчин в возрасте старше 40 лет, страдающих заболеваниями мочеполовой и сердечно-сосудистой систем и находившихся на лечении в городской клинической урологической больнице № 47 Департамента здравоохранения г. Москвы. При этом больных с сочетанием ИБС и гипертонической болезни было 60%, с гипертонической болезнью – 20%, с ИБС и стенокардией I и II ФК – 20%. В зависимости от основного диагноза больным были произведены: трансуретральная резекция предстательной железы, дистанционная литотрипсия, нефрэктомия, радикальная простатэктомия и некоторые другие оперативные вмешательства. Все больные на предоперационном этапе прошли холтеровское мониторирование (ХМЭКГ) и были проконсультированы кардиологом. Впослеоперационном периоде, на 2‑е и 10‑е сутки, проводили повторный осмотр кардиологом и ХМ-ЭКГ; при необходимости корректировали кардиотропную терапию.
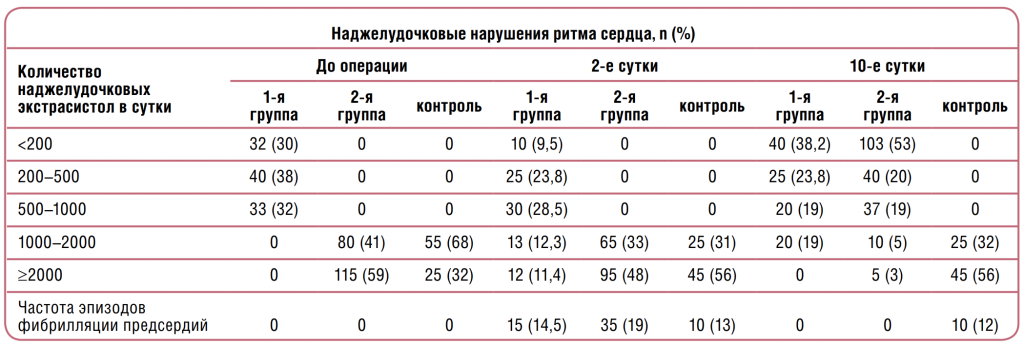
В исследование не включали больных, страдающих постоянной и пароксизмальной формами фибрилляции предсердий, а также постоянно получающих β-адреноблокаторы. У всех больных при ХМ-ЭКГ был зарегистрирован синусовый ритм со средней частотой сердечных сокращений за сутки от 58 до 85 в минуту и наджелудочковые нарушения ритма сердца (см. таблицу). С учетом количества зарегистрированных экстрасистол больные были разделены на 2 группы: в 1‑ю вошли больные (n=105) с исходным количеством наджелудочковых экстрасистол <1000 в сутки, во 2‑ю (n=195) – 1000 и более экстрасистол. Всем больным 2‑й группы до оперативного вмешательства были назначены метопролол (50–100 мг/сут) и Панангин (по 2 таблетки 3 раза в день в течение 1‑й недели лечения, в последующие 5 нед – по 1 таблетке 3 раза в сутки). Для оценки эффективности терапии ретроспективно была составлена контрольная группа (пациенты с аналогичными урологическими заболеваниями и исходным количеством наджелудочковых экстрасистол >1000 в сутки). В контрольной группе плановую терапию не проводили. При необходимости назначали амиодарон для купирования пароксизмов фибрилляции предсердий. На 2‑е сутки после оперативного вмешательства в 1‑й группе пароксизмы фибрилляции предсердий были выявлены у 15 (14,5%) больных, причем пароксизмы оказались кратковременными и купировались самостоятельно. Среди остальных 90 пациентов этой группы у 9,5% пациентов отмечено <200 наджелудочковых экстрасистол в сутки, у 23,8% – от 200 до 500, у 8,5% больных – 500–1000 и у 2,7% пациентов – более 1000 в сутки. Больным 1‑й группы дополнительное медикаментозное лечение не назначали. Несмотря на проводимую терапию, на 2‑е сутки после операции у 19% пациентов 2‑й группы при ХМ-ЭКГ были зарегистрированы пароксизмы фибрилляции предсердий, причем в 87% случаев указанные нарушения ритма были кратковременными и купировались самостоятельно, а в 13% случаев потребовали введения амиодарона. У остальных 81% больных пароксизмов фибрилляции предсердий не отмечено, однако зарегистрировано >1000 наджелудочковых экстрасистол в сутки. На 10‑е сутки после операции на фоне терапии эпизоды фибрилляции предсердий не регистрировали, а число больных с количеством наджелудочковых экстрасистол >1000 в сутки уменьшилось до 8%. В контрольной группе, в которой превентивную терапию метопрололом и Панангином не проводили, на 2‑е сутки после оперативного вмешательства регистрировали такие же нарушения ритма и с такой же частотой, как и в основной группе. Статистически достоверных различий не обнаружено. Однако на 10‑й день после оперативного вмешательства количество наджелудочковых экстрасистол >1000 в сутки отмечено у 88% больных контрольной группы, что достоверно выше, чем в основной (8%). Кроме того, у 12% пациентов контрольной группы на 10‑й день после операции зарегистрированы пароксизмы фибрилляции предсердий, которых не было у больных, получавших терапию метопрололом и Панангином. Проведенное нами исследование показало, что при сочетанной урологической и кардиологической патологии Панангин в составе комплексной терапии характеризуется высокой клинической эффективностью в профилактике послеоперационных аритмий. Учитывая нередко встречающееся у урологических больных нарушение функции почек, необходимо обращать особое внимание на возможные противопоказания к назначению препаратов, содержащих калий и магний: гипермагниемия, хроническая почечная недостаточность III стадии (терминальная), мочекаменная болезнь, если магний входит в состав почечных конкрементов, кетоацидоз, выраженная брадикардия, атриовентрикулярная блокада II–III степени. Отметим, что негативное влияние на течение нефролитиаза возможно только при длительном (многонедельном) приеме препаратов магния. Кратковременные курсы в послеоперационном периоде, направленные на предотвращение аритмии, по нашему мнению, вполне возможны при любой форме мочекаменной болезни. Очевидно, что в данной клинической ситуации риск развития суправентрикулярной аритмии и фибрилляции предсердий значительно выше, чем возможность рецидирования нефролитиаза. Следует помнить, что только врач способен определить необходимость назначения лекарственного препарата, даже такого относительно безопасного, как Панангин. Повышение уровня калия в крови >5 ммоль/л вызывает настороженность, уровень калия в крови >5,5 ммоль/л может представлять угрозу для жизни и требует немедленного медицинского вмешательства. Таким образом, Панангин можно применять в схеме терапии и профилактики наджелудочковых аритмий, в том числе и после урологических оперативных вмешательств.
1. Костюченко Л. Н. Нарушения калий-магниевого гомеостаза и его коррекция в ходе нутриционной поддержки больных гастроэнтерологического профиля // Трудный пациент. – 2010; 10 (8): 40–47.
2. Агаджаняна Н. А., Циркина В. И. Физиология человека. – Спб.: Сотис, 1998. – 528 с.
3. Кудрин А.В., Громова О.А. Микроэлементы в неврологии.– М.: 2006.– 303 с.
4. Лазебник Л. Б., Дроздова С. Л. Коррекция магниевого дефицита при сердечно-сосудистой патологии. Кардиология. – 1997;
5. – С. 103–104. 5. Орлов В.И. Руководство по электрокардиографии.– М., 1998.– 67 с.
6. Ascherio A., Rimm E., Hernan M. Intake of potassium, magnesium, calcium and fiber and risk of stroke among US men. // Circulation.– 1998, 98, 1198–1204.
7. Ekmekci O., Donma O., Tunckale A. Angiotensin-converting enzyme and metals in untreated essential hypertension // Biol. Trace Elem. Res.– 2003; 3: 203–210.
8. Whang R., Whang D., Ryan M. Refractory potassium repletion: a consequence of magnesium deficiency // Arch. Intern. Med.– 1992; 152: 40–45.
9. Liao F., Folsom A., Brancati F. Is low magnesium concentration a risk factor of coronary heart disease? The Atherosclerosis Risk in Communities (ARIC) Study // Am. Heart J. – 1998; 136 (3): 480–490.
10. Ueshima K. Magnesium and ischemic heart disease: a review of epidemiological, experimental and clinical evidences // Magnes Res.– 2005; 95 (3): 203–210.
11. He F., MacGregor G. Potassium intake and blood pressure // Am.J. Hypertens.– 1999; 12: 849–851
12. Ma B., Lawson A., Liese A. Dairy, magnesium and calcium intake in relation to insulin sensitivity: approaches to modeling a dose – dependent association // Am. J. Epidemiol. – 2006; 164 (5): 449–458.
13. Iezhitsa I. Potassium and magnesium depletions in congestive heart failure – patophysiology, consequences and replenishment // Clin Calcium. – 2005; 15 (11): 123–133.
14. Shechter M., Sharir M., Labrador M. Oral magnesium therapy improves endothelial function in patients with coronary artery disease // Circulation. – 2000; 102: 2353–2358.
15. Roberts D., Buckley N. Antidotes for acute cardenolide (cardiac glycoside) poisoning. Cochrane Database Syst Rev. – 2006; 18 (4): CD005490.
16. Рогозина Н. П., Чурин К. В., Чурина С. К. Пероральные препараты магния при остром инфаркте миокарда: влияние на течение заболевания и развитие аритмий // Вестн. аритмологии. – 2000; 19: 23–28.
17. Gottlieb S., Baruch L., Kukin M. Prognostic importance of the serum magnesium concentration in patients with congestive heart failure // J. Am. Coll. Cardiol. – 1990; 16: 827–831.
18. Hadj A., Pepe S., Marasco S. et al. The principles of metabolic therapy for heart disease // Heart. Lung. Circ. – 2003; 12 (2): 55–62.
19. Choy A., Lang C., Chomsky D. Normalization of acquired QT prolongation in humans by intravenous potassium // Circulation. – 1997; 96: 2149–2154.
20. Nolan J., Batin P., Andrews R. Prospective study of heart rate variability and mortality in chronic heart failure: results of the Unit===ed Kingdom heart failure evaluation and assessment of risk trial (UK- heart) // Circulation. – 1998; 98: 1510–1516.
21. Zehender M., Meinertz T., Just H. Magnesium deficiency and magnesium substitution. Effect of ventricular cardiac arrhythmias of various etiology // Herz. – 1997; 22 (1): 56–62.
ELECTROLYTE DISORDERS AND THEIR CORRECTION S. Davydova, Candidate of Medical Sciences; I. Komissarenko, MD City Clinical Urology Hospital Forty-Seven, Central Gastroenterology Research Institute, Moscow The paper considers electrolyte disorders in gastroenterology and gives the results of using panangin and the β-adrenoblocker metoprolol in the prevention and treatment of supraventricular tachyarrhythmia after operations on the urinary system in patients with concomitant cardiac and urologic problems. Key words: potassium, magnesium, panangin, supraventricular tachycardia, premature supraventricular contractions, urologic surgical interventions