Роль Панангина в лечении острого инфаркта миокарда
Хэ Гуэйсинь (Больница Жуйкан, Университет традиционной китайской медицины Гуанси, Наньнин, 530011, Китай)

Низкий уровень магния может вызывать структурные и функциональные нарушения со стороны сердечно-сосудистой системы, приводящие к потенцированию некроза миокарда, кальцификации или спазму коронарной артерии. В то же время низкий уровень магния также тесно связан с тяжелой аритмией и сердечной недостаточностью [1], а нарушение обмена калия может вызывать аритмию и влиять на диастолическую функцию миокарда [2]. Для дополнительной оценки роли препаратов калия и магния в лечении острого инфаркта миокарда (ОИМ), автор данной статьи назначал Панангин 40 пациентам с ОИМ, поступившим в отделение интенсивной терапии в нашей больнице с 1998 года, и сравнил с 40 пациентами, получавшими традиционное лечение. Результаты исследования представлены ниже.
1. Материалы исследования.
1.1 Общая информация о пациентах.
80 пациентам в соответствии с диагностическими критериями ВОЗ был поставлен диагноз острый инфаркт миокарда. Все пациенты были госпитализированы в отделение реанимации, в срок менее трех дней от начала заболевания, при поступлении в стационар у пациентов отсутствовали суправентрикулярная тахикардия, вентрикулярная экстрасистолия, желудочковая тахикардия, фибрилляция желудочков, также не наблюдалось кардиогенного шока и сердечной недостаточности выше III ФК. Сопутствующие (коморбидные) заболевания, такие как церебральная и почечная недостаточность, гиперкалиемия отсутствовали. Пациенты были разделены на две группы по принципу случайной выборки. В группе лечения Панангином было 40 пациентов, 30 мужчин и 10 женщин, возраст (58,24 ±11,23) лет. Местоположения инфаркта: 16 случаев инфаркта миокарда передней стенки, 12 случаев инфаркта миокарда задней стенки, 6 случаев инфаркта миокарда боковой стенки, 6 случаев субэндокардиального инфаркта миокарда. В контрольной группе также было 40 пациентов, 28 мужчин и 12 женщин, возраст (61,58 ± 9,55) лет, локализация инфаркта — 14 случаев инфаркта миокарда передней стенки, 13 случаев инфаркта миокарда задней стенки, 7 случаев инфаркта миокарда боковой стенки и 6 случаев субэндокардиального инфаркта миокарда. Распределение по возрасту, гендерному составу и локализации инфаркта миокарда в обеих группах было схожим. Обе группы были сопоставимы, без наличия значимых различий (P> 0,05).
1.2 Методы лечения.
2 группы лечились в соответствии со стандартной схемой лечения ОИМ, применялись такие методы как внутривенный тромболизис, стентирование, использовались средства, снижающие потребность миокарда в кислороде, статины, антикоагулянты, антиагреганты, ИАПФ, при выявлении желудочковой экстрасистолии ниже второй степени по классификации (градации) Лауна-Вольфа профилактическая терапия лидокаином не применялась. Исходя из этого, основной группе давали инъекции Панангина по 40 мл (производимой ОАО «Гедеон Рихтер», Будапешт) плюс 500 мл 5% раствора глюкозы и вводили внутривенно со скоростью 4 мл / мин один раз в день. Дополнительно Панангин давали перорально по 2 таблетки 3 раза в сутки, в течение 2-х недель. Контрольной группе давали поляризующий раствор: 500 10% глюкозы мл + 10 мл 10% раствора хлорида калия + 10 мл 25% сульфата магния + обычный инсулин 8 МЕ, 1 раз / сут, 2 недели — 1 курс лечения. В течение первых трех дней после поступления в стационар было выполнено 6 энзимограмм миокарда. Каждые 30 минут или каждый час проверяли ЭКГ по 12 отведениям, делали анализы на количество калия в крови, лечение в палате реанимации проходило в течение 1 недели. После 1 недели терапии, контроля ЭКГ с мониторингом артериального давления и дыхательной функции больных переводили в общее отделение на 1 неделю. В среднем период госпитализации пациентов занимал 3-4 недели, при выписке были зафиксированы улучшения сердечной функции и явное снижение симптомов аритмии.
2. Результаты
2.1 Случаи аритмии в двух группах лечения.
В группе лечения Панангином было 2 случая суправентрикулярной (наджелудочковой) тахикардии, в 5 случаях наблюдалась желудочковая экстрасистолия, в 2 случаях желудочковая тахикардия и в 1 случае фибрилляция жуледочков. Случаи аритмии были зарегистрированы у 25% пациентов.
В группе лечения поляризующей смесью было зарегистрировано 4 случая развития суправентрикулярной (наджелудочковой) тахикардии, 11 случаев желудочковой экстрасистолии, 8 случаев желудочковой тахикардии, 3 случая фибрилляции желудочков, суммарно аритмия развивалась у 65% пациентов. Частота возникновения аритмии между двумя группами имела достоверные различия: (P <0,01).
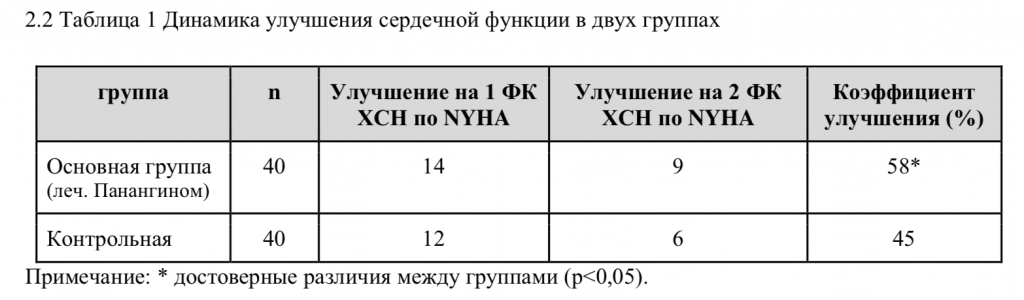
3. Обсуждение результатов
Панангин — это торговое наименование аспарагината калия-магния, комбинации солей калия и магния аспарагинатов, выпускается для инъекций 10 мл / ампула, содержащая 0,4 г аспарагината магния (33,70мг Mg2 +) и 0,425 г аспарагината калия (103,30мг K+), и в форме таблеток. Аспарагиновая кислота — это аминокислота с высоким сродством (аффинностью) к клеткам, она образует прочные комплексные соединения с ионами металлов K + и Mg2 +. Аспарагиновая кислота обладает выраженной тропностью к клеткам и может быть использована в качестве «носителя» для переноса ионов калия и магния в клетки. В то же время аспарагиновая кислота участвует в цикле орнитина, цикле трикарбоновых кислот и процессе генерации внутриклеточного АТФ. Таким образом, клиническое применение Панангина в качестве донатора ионов калия и магния для лечения ССЗ более оправдано чем хлорид калия, сульфат магния и поляризующей смеси. Результаты этого исследования показали, что по сравнению с контрольной группой, в острой фазе (<30 дней) частота тяжелой аритмии в группе лечения Панангином была существенно ниже, улучшение сердечной функции было более очевидным, а разница между группами была статистически значимой. Отсюда следует вывод, что Панангин оказывает ощутимое клиническое действие в острой фазе лечения ОИМ.
Калий является важным внутриклеточным катионом. Ионы калия участвуют в регуляции электрохимического состояния мембраны кардиомиоцитов, проведении электрических импульсов, поддерживают сократительную функцию миокарда и уменьшают потребление кислорода миокардом. Магний является коферментом Na+, K+-АТФазы в кардиомиоцитах. Магний регулирует активность различных ферментов, в т.ч. управляющих током ионов калия, магний способен предотвращать потерю калия клетками, тем самым поддерживая его высокий внутриклеточный уровень, стабилизировать потенциал покоя, устраняя аритмию. Ионы магния также непосредственно влияют на кардиомиоциты, замедляют атриовентрикулярную проводимость, продлевают период абсолютной рефрактерности, снижают возбудимость кардиомиоцитов и препятствуют формированию повторного входа волны возбуждения (re-entry). Следовательно, Панангин обладает хорошим антиаритмическим потенциалом [3-4]. Данное исследование показало, что по сравнению с контрольной группой частота возникновения злокачественных аритмий в группе лечения Панангином была значительно ниже, причем разница была достоверной (Р <0,01), что указывает на то, что Панангин действительно обладает убедительной антиаритмической активностью. Во время ОИМ в миокарде наблюдается массивный коагуляционный некроз, интерстициальный застой и отек миокарда, сопровождающийся воспалительной инфильтрацией. В это же время наблюдаются гемодинамические изменения в левом желудочке, снижается сократимость миокарда, снижается податливость стенок миокарда,сразу же снижается ударный объем сердца, сердечный выброс, и происходит тяжелая недостаточность насосной функции [5].
Mg2 + и K + являются основными катионами в клетке. Магний является ко-фактором множества различных ферментов. Например, магний необходим для активации Na +, K + -АТФазы и аденилатциклазы, что играет важную роль в поддержании митохондриальной функции кардиомиоцитов. Магний способствует интенсификации и облегчению окислительного фосфорилирования, оказывает дилатирующее действие на коронарные артерии, уменьшает нагрузку на сердце, уменьшает ишемию миокарда [6]. В то же время магний, действуя как ко- фактор Na +, K + -АТФазы, защищает клетки миокарда от потери калия. Калий так же является важным дополнительным компонентом для синтеза высокоэнергетических фосфатных соединений (АТФ), необходимых для поддержания моторной функцию миокарда и снижения потребности миокардом в кислороде [7]. Следовательно, при лечении острой сердечной недостаточности при инфаркте миокарда добавление ионов калия и магния может не только улучшить метаболизм, повысить сократительную способность, но также снизить ишемию миокарда. Панангин содержит аспарагинаты магния и калия. Аспарагиновая кислота обладает сильным сродством к клеткам. Она может использоваться в качестве носителя K + и Mg2 + для транспорта ионов сквозь клеточные мембраны и увеличения внутриклеточного содержания ионов магния и калия. Добавки препаратов K + и Mg2 + могут стабилизировать мембранный потенциал, предотвращать аритмию, улучшать сократимость и диастолическую функцию миокарда, снижать потребление кислорода и способствовать восстановлению сердечной функции. Это исследование показывает, что Панангин может значительно улучшать функциональность миокарда, обладая значительно лучшим и надежным эффектом, чем поляризующая смесь. В заключение необходимо отметить, что Панангин может значительно снизить частоту возникновения аритмии при лечении ОИМ и улучшить сердечную функцию. Терапевтический эффект Панангина является стабильным и легко прогнозируемым, терапия сопровождается малым числом нежелательных явлений, поэтому Панангин можно использовать как препарат для комплексной терапии ОИМ, заслуживающий широкого клинического применения.
3. Обсуждение результатов
Панангин — это торговое наименование аспарагината калия-магния, комбинации солей калия и магния аспарагинатов, выпускается для инъекций 10 мл / ампула, содержащая 0,4 г аспарагината магния (33,70мг Mg2 +) и 0,425 г аспарагината калия (103,30мг K+), и в форме таблеток. Аспарагиновая кислота — это аминокислота с высоким сродством (аффинностью) к клеткам, она образует прочные комплексные соединения с ионами металлов K + и Mg2 +. Аспарагиновая кислота обладает выраженной тропностью к клеткам и может быть использована в качестве «носителя» для переноса ионов калия и магния в клетки. В то же время аспарагиновая кислота участвует в цикле орнитина, цикле трикарбоновых кислот и процессе генерации внутриклеточного АТФ. Таким образом, клиническое применение Панангина в качестве донатора ионов калия и магния для лечения ССЗ более оправдано чем хлорид калия, сульфат магния и поляризующей смеси. Результаты этого исследования показали, что по сравнению с контрольной группой, в острой фазе (<30 дней) частота тяжелой аритмии в группе лечения Панангином была существенно ниже, улучшение сердечной функции было более очевидным, а разница между группами была статистически значимой. Отсюда следует вывод, что Панангин оказывает ощутимое клиническое действие в острой фазе лечения ОИМ.
Калий является важным внутриклеточным катионом. Ионы калия участвуют в регуляции электрохимического состояния мембраны кардиомиоцитов, проведении электрических импульсов, поддерживают сократительную функцию миокарда и уменьшают потребление кислорода миокардом. Магний является коферментом Na+, K+-АТФазы в кардиомиоцитах. Магний регулирует активность различных ферментов, в т.ч. управляющих током ионов калия, магний способен предотвращать потерю калия клетками, тем самым поддерживая его высокий внутриклеточный уровень, стабилизировать потенциал покоя, устраняя аритмию. Ионы магния также непосредственно влияют на кардиомиоциты, замедляют атриовентрикулярную проводимость, продлевают период абсолютной рефрактерности, снижают возбудимость кардиомиоцитов и препятствуют формированию повторного входа волны возбуждения (re-entry). Следовательно, Панангин обладает хорошим антиаритмическим потенциалом [3-4]. Данное исследование показало, что по сравнению с контрольной группой частота возникновения злокачественных аритмий в группе лечения Панангином была значительно ниже, причем разница была достоверной (Р <0,01), что указывает на то, что Панангин действительно обладает убедительной антиаритмической активностью. Во время ОИМ в миокарде наблюдается массивный коагуляционный некроз, интерстициальный застой и отек миокарда, сопровождающийся воспалительной инфильтрацией. В это же время наблюдаются гемодинамические изменения в левом желудочке, снижается сократимость миокарда, снижается податливость стенок миокарда, сразу же снижается ударный объем сердца, сердечный выброс, и происходит тяжелая недостаточность насосной функции [5].
Mg2 + и K + являются основными катионами в клетке. Магний является ко-фактором множества различных ферментов. Например, магний необходим для активации Na +, K + -АТФазы и аденилатциклазы, что играет важную роль в поддержании митохондриальной функции кардиомиоцитов. Магний способствует интенсификации и облегчению окислительного фосфорилирования, оказывает дилатирующее действие на коронарные артерии, уменьшает нагрузку на сердце, уменьшает ишемию миокарда [6]. В то же время магний, действуя как ко- фактор Na +, K + -АТФазы, защищает клетки миокарда от потери калия. Калий так же является важным дополнительным компонентом для синтеза высокоэнергетических фосфатных соединений (АТФ), необходимых для поддержания моторной функцию миокарда и снижения потребности миокардом в кислороде [7]. Следовательно, при лечении острой сердечной недостаточности при инфаркте миокарда добавление ионов калия и магния может не только улучшить метаболизм, повысить сократительную способность, но также снизить ишемию миокарда. Панангин содержит аспарагинаты магния и калия. Аспарагиновая кислота обладает сильным сродством к клеткам. Она может использоваться в качестве носителя K + и Mg2 + для транспорта ионов сквозь клеточные мембраны и увеличения внутриклеточного содержания ионов магния и калия. Добавки препаратов K + и Mg2 + могут стабилизировать мембранный потенциал, предотвращать аритмию, улучшать сократимость и диастолическую функцию миокарда, снижать потребление кислорода и способствовать восстановлению сердечной функции. Это исследование показывает, что Панангин может значительно улучшать функциональность миокарда, обладая значительно лучшим и надежным эффектом, чем поляризующая смесь. В заключение необходимо отметить, что Панангин может значительно снизить частоту возникновения аритмии при лечении ОИМ и улучшить сердечную функцию. Терапевтический эффект Панангина является стабильным и легко прогнозируемым, терапия сопровождается малым числом нежелательных явлений, поэтому Панангин можно использовать как препарат для комплексной терапии ОИМ, заслуживающий широкого клинического применения.
Шао Мэйчжэнь, Ло Дечэн. Основные характеристики магния и клиническое лечение [M]. Чэнду:
Сычуаньская Наука и Технология, 1988: 245-248
Дай Цзыин. Практическая медицина внутренних болезней. [M] .8 издание. Пекин: Народное
медицинское издательство, 1996: 588.
Силинг М.С. Сердечно-сосудистые последствия дефицита магния
и проблемы: патогенез: распространенность и проявления - магний и
потеря хлорида в рефракторном калии [J]. Am J Cardiol, 1989, 63: 4-21
Ван Х. Частота гипомагниемии у госпитализированных больных, получающих дигиталис [J]. Arch
Intern Med, 1985, 145: 655
Чэнь Ючжу. Практическая медицина внутренних органов [M] .11. Пекин: Народный медицинский
издательский дом, 2001: 1381-1382
Чжэн Хуэй, Лин Югуан, Ли Ифэн и др. Применение аспартата калия и магния в кардиохирургии [J].
Китайский журнал сердечно-сосудистых заболеваний, 1996, 24 (1): 31-32
Цзя Сюйхун. Дефицит магния и сердечная недостаточность [J]. Foreign Medical Pediatrics, 1993, 20
(6): 298
[Номер CLC] R0542.22 [Код документа] A [Код статьи] 1008-8849 (2005) 14 -1821 -02
Статья подготовлена по переведенным материалам, находившимся в открытом доступе на портале https://www.cnki.net/ *
*Китайская национальная инфраструктура знаний (China National Knowledge Infrastructure, CNKI) – глобальный информационный проект Китайской Народной Республики (КНР), университета Циньхуа (Пекин) и холдинга Tsinghua Tongfang, начатый в 1996 году. Университет Циньхуа (основан в 1911 году) — ведущий университет Китая. По данным официального портала CNKI, в настоящее время пользователями CNKI являются более 1500 университетов, научно- исследовательских институтов, правительственных организаций, компаний и предприятий в 53 странах мира, в том числе в России, и более 25 тысяч организаций в самом Китае.